Por Graham Bilbrough, Barbara Evert, Karen Hathaway, Gina Panagakos, Jane Robertson y Maha Yerramilli
INSTRODUCCIÓN
La SDMA es una forma metilada de la arginina, que se encuentra en las proteínas intracelulares de todas las células nucleadas de los vertebrados y se excreta a través de los riñones. La SDMA se correlaciona favorablemente con la tasa de filtración glomerular (TFG) en personas,1 perros,2,3 y gatos. 4–6 La SDMA es más sensible y aumenta antes que la creatinina (CREA). La creatinina no aumenta por encima del rango de referencia hasta que se pierde el 75% de la función renal, los estudios han demostrado que la SDMA aumenta cuando hay una disminución de la tasa de filtración glomerular (TFG) media del 40% y con tan sólo un 25% en su disminución.2,3,5 La SDMA aumenta tanto en la lesión renal aguda o activa como con la enfermedad renal crónica, lo que permite a los veterinarios intervenir antes y obtener resultados más satisfactorios en los paciente. Además, la SDMA, a diferencia de la CREA, no se ve afectada por la masa muscular.6,7 Por estas razones, la prueba IDEXX SDMA® se convierte rápidamente en un parámetro esencial en todos los perfiles químicos de rutina.
La prueba SDMA en el Catalyst es un nuevo sistema de inmunoensayo de IDEXX que está diseñado para medir las concentraciones de SDMA en muestras de suero o plasma de heparina de litio de perros y gatos sin necesidad de diluir la muestra. Está diseñado para producir resultados de pruebas rápidos, fiables y precisos en la clínica veterinaria tanto en el analizador químico IDEXX Catalyst One® como en el IDEXX Catalyst Dx®. Estos tienen el mismo rango de referencia (0-14 µg/dL), pautas de interpretación e intervalo de lectura (0-100 µg/dL) que la prueba de laboratorio de referencia IDEXX SDMA.
LOS CUATRO OBJETIVOS DE ESTE ESTUDIO ERAN EVALUAR:
- Rendimiento de la nueva prueba mediante una comparación de métodos con un método de referencia (comparación de métodos).
- Precisión de la prueba utilizando fluidos de control (precisión).
- Especificidad analítica (especificidad análoga).
- Impacto de la hemólisis, la lipemia y la ictericia en la concentración notificada (substancias que interfieren).
MATERIALES Y MÉTODOS
Los datos se cotejaron en Microsoft Office Excel® 2016* antes de exportarlos a JMP® 13.0.0† para su análisis estadístico, incluido el complemento de comparación de métodos‡.
Comparación de métodos
Se recogieron muestras de suero residual de 107 perros y 113 gatos, incluyendo una mezcla de animales sanos y pacientes clínicos.
Todas las muestras se analizaron una vez con la prueba IDEXX Catalyst® SDMA y dos veces con un método analítico de cromatografía líquida – espectrometría de masas (LC-MS).§ El promedio de los resultados de LC-MS se tomó como método de referencia y se comparó con los resultados de la prueba IDEXX Catalyst SDMA.
Se completó el análisis de regresión lineal de Passing-Bablok para cada especie. Los coeficientes de correlación se interpretaron como aparece a continuación: r = 0,90-1,0, definida como correlación muy alta; 0,70-0,89, correlación alta; 0,50-0,69, correlación moderada; 0,30-0,49, correlación baja; y 0-0,29, correlación escasa o nula.8
El análisis de regresión también se utilizó para buscar pruebas estadísticas de error sistemático (sesgo constante y/o proporcional). Los intervalos de confianza (IC) del 95% para la intersección y que no incluían el valor cero se consideraron como evidencia de un sesgo constante. Los IC del 95% para la pendiente que no incluían el valor 1,0 se consideraron como evidencia de sesgo proporcional.
Los resultados de cada método, aproximados al numero entero, fueron clasificados en los siguientes rangos: £14 µg/dL (dentro del intervalo de referencia); 15-19 µg/dL; ³20 µg/dL. A continuación, se compararon las clasificaciones en una tabla de contingencia para cada especie.
PRECISIÓN
La precisión se valoró según las directrices del método EP5-A del Instituto de Normas Clínicas y de Laboratorio (CLSI por sus iniciales en inglés).9Se analizaron dos niveles de fluidos de control (fluido A y fluido B) en un Analizador Químico Catalyst Dx. Para cada especie, se realizaron 4 repeticiones cada mañana y cada tarde durante 10 días, lo que supone un total de 80 réplicas por especie. La precisión total se calculó según las directrices del método CLSI EP5-A.
*Microsoft Office Excel® 2016, Microsoft Corporation, Redmond, Washington, EEUU.†JMP® 13.0.0, SAS Institute Inc. Cary, Carolina del Norte, EEUU.‡Method Comparison Add-in, SAS Institute Inc. Cary, Carolina del Norte, EEUU.§El método LC-MS se describió en un resumen de la AACC 2015. La separation en LC se logró utilizando la columna de fase inversa Xbridge™ reverse-phase (RP) C18 y un agende de emparejamiento de iones. El espectrómetro de masas de triple cuadrupolo API 4000™ (Applied Biosystems/MDS Sciex) funcionó en modo de monitorización de reacciones múltiples (MRM) con interfaz de electrospray positivo. La transición MRM para la DMAS se observó a m/z 203.2 ➔ 172.1.10
ESPECIFICIDAD ANÁLOGA
Las pruebas de reacción cruzada se completaron añadiendo tres materiales de control diferentes con concentraciones fisiológicamente relevantes de arginina, dimetilarginina asimétrica (DMAS) o monometil-L-arginina (MMA). PBS (phosphate buffer solution o solución reguladora de fosfatos) se utilizó como control para compensar el cambio de volumen con el aditivo (“control”).
Para cada fluido de control, había cuatro alícuotas (enriquecidas con ADMA, enriquecidas con MMA, enriquecidas con arginina y “control”), dando un total de 12 alícuotas que se analizaron seis veces cada una con la prueba SDMA de IDEXX en el Catalyst y se calculó una media.

La concentración media de la SDMA “enriquecida” para cada alícuota se comparó con la concentración media de la SDMA “de control” para buscar una diferencia estadísticamente significativa (Tukey-Kramer HSD; P<0,05).
SUSTANCIAS INTERFERENTES
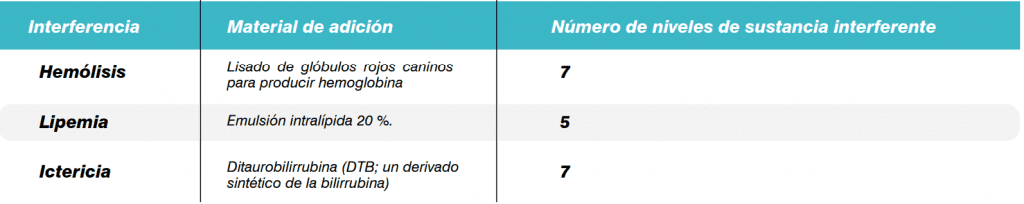
Las interferencias causadas por la presencia de hemoglobina, lípidos o bilirrubina se evaluaron según las directrices del método CLSI EP7-A2.11 Las muestras de suero canino, que estaban visiblemente libres de interferencias, se recogieron y agruparon. A continuación, se prepararon alícuotas de la muestra combinada y se les añadieron concentraciones variables de las sustancias indicadas en la tabla 1. Cada alícuota se analizo por duplicado en ocho analizadores químicos Catalyst One en un orden aleatorio.
Tabla 1. Preparación de alícuotas de la muestra colectiva para evaluar las sustancias interferentes comunes.
Se realizó una prueba HSD de Tukey-Kramer de todos los pares (P<0,05) con la concentración media de la SDMA de cada alícuota para buscar diferencias estadísticamente significativas.
RESULTADOS
Comparación de métodos.
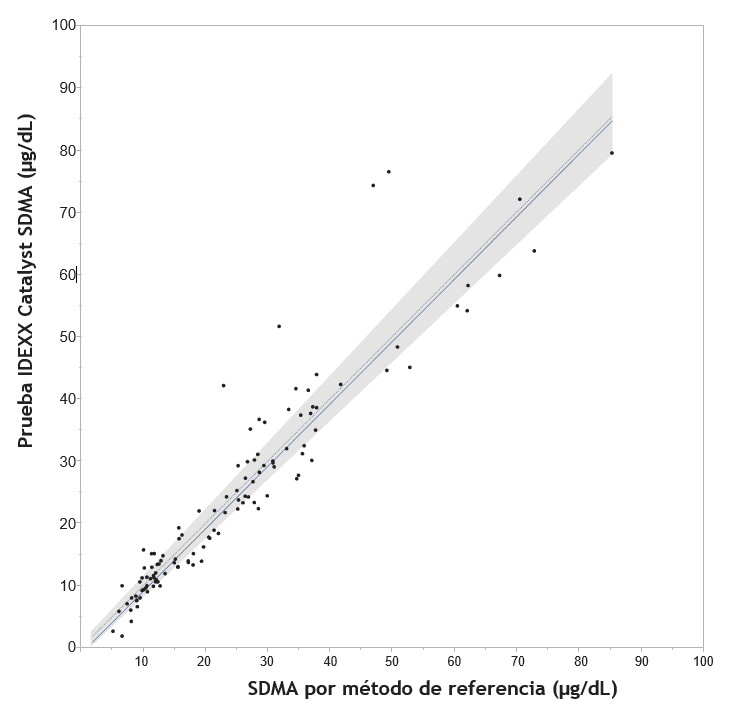
Los gráficos de regresión se muestran en las figuras 1A (canina) y 1B (felina). Los resultados se resumen en las tablas 2 y 3. La Prueba IDEXX Catalyst® SDMA mostró una excelente correlación con el método de referencia, sin evidencia de sesgo para ninguna de las dos especies. En cuanto a la clasificación de los resultados, hubo una gran coincidencia entre los dos métodos.
Figura 1. Regresión Passing–Bablok.
La línea de regresión se muestra en azul (con un IC del 95%); la unidad se muestra como línea discontinua gris.
A. Caninos: n = 107; correlación (r) = 0,98; pendiente = 0,98; intercepción = 0,44 µg/dL
B. Felinos: n = 113; correlación (r) = 0,94; pendiente = 1,00; intercepción = -0,95 µg/dL
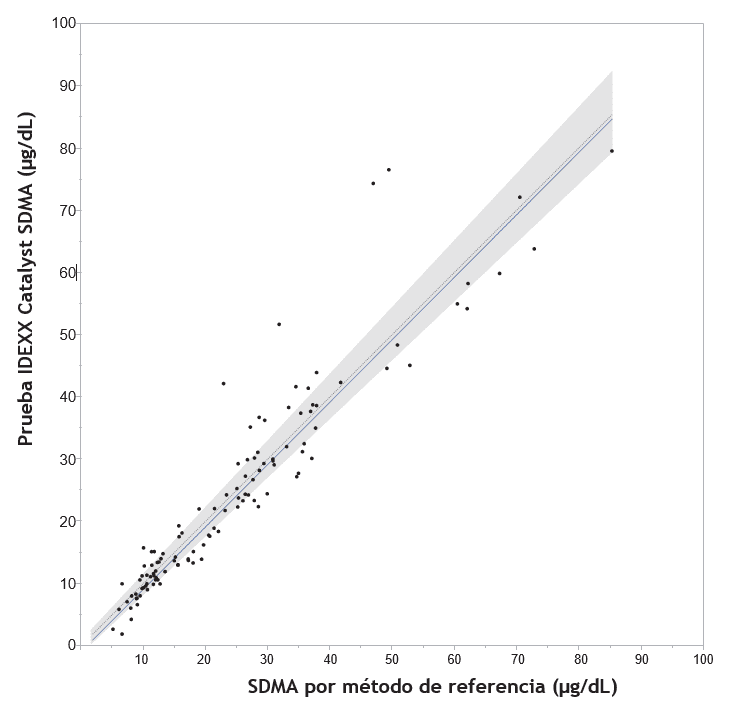
Tabla 2. Análisis de regresión por especies.
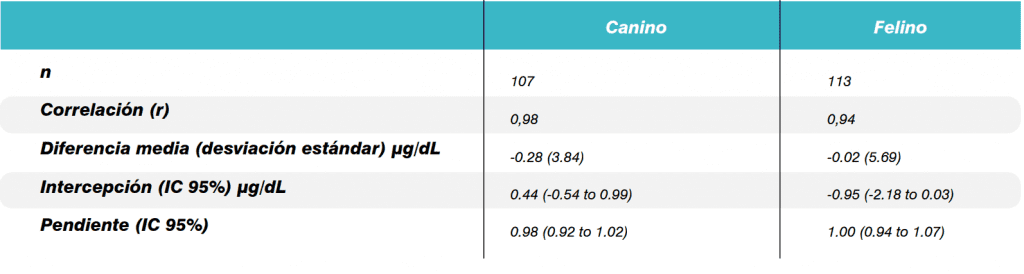
Tabla 3. Tabla de contingencia por especies.
A. Caninos: n = 107; concordancia global = 95%.
Resultado de la Prueba Catalyst SDMA
Concentración media de SDMA según el método de referencia
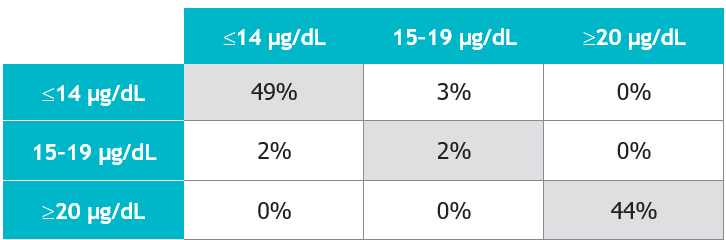
Para las muestras discordantes, la diferencia absoluta media fue de 2 µg/dL.
B. Felinos: n = 113; concordancia global = 85%.
Resultado de la Prueba Catalyst SDMA
Concentración media de SDMA según el método de referencia
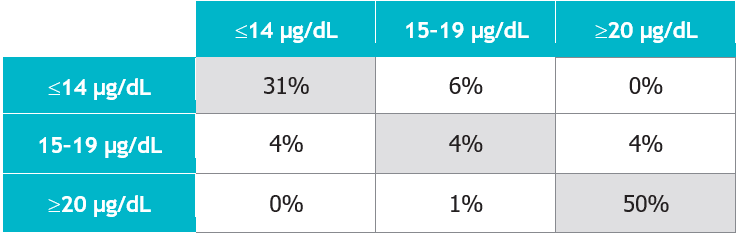
Para las muestras discordantes, la diferencia absoluta media fue de 3 µg/dL.
PRECISIÓN
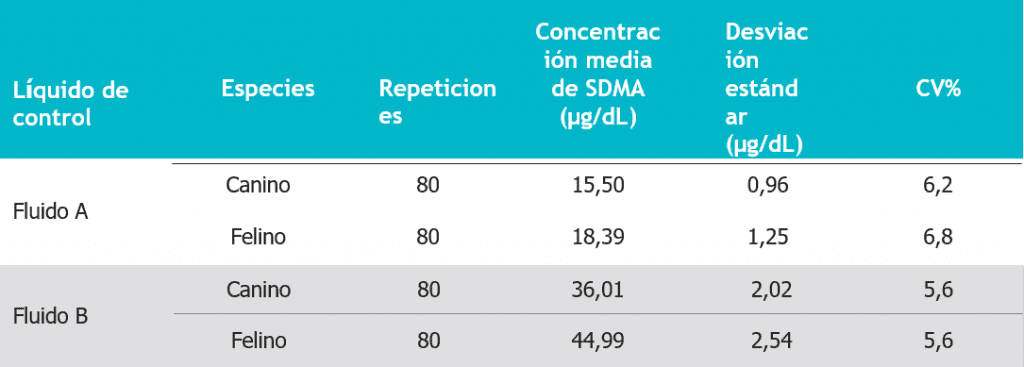
Los resultados del análisis de precisión se muestran en la tabla 4. El nuevo método muestra un coeficiente de variación (CV) total de <10%. Esto es coherente con el inmunoensayo de alto rendimiento para la SDMA utilizado en los Laboratorios de Referencia IDEXX.¶
Tabla 4. Resumen de los resultados del estudio de precisión.
ESPECIFICIDAD ANÁLOGA
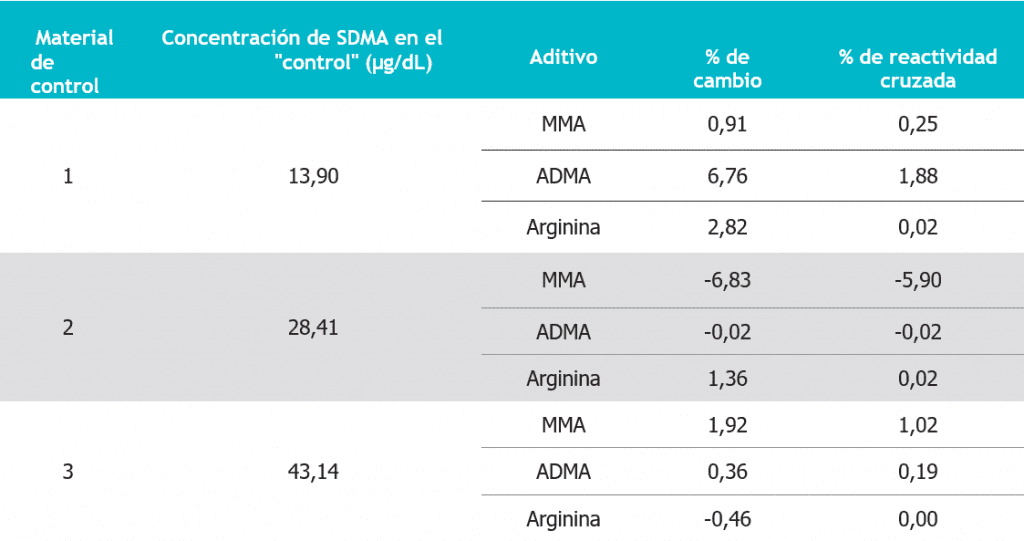
Los resultados del análisis de especificidad se muestran en la tabla 5. No se observaron cambios estadísticamente significativos con ninguna de las alícuotas enriquecidas.
Tabla 5. Resumen del estudio de especificidad análoga. Concentración del aditivo después de su enriquecimiento: MMA 50 µg/dL; ADMA 50 µg/dL; arginina 2.500 µg/dL.
¶Un resumen de la AACC 2015 mostró que la precisión total era del £10%.12
SUSTANCIAS INTERFERENTES
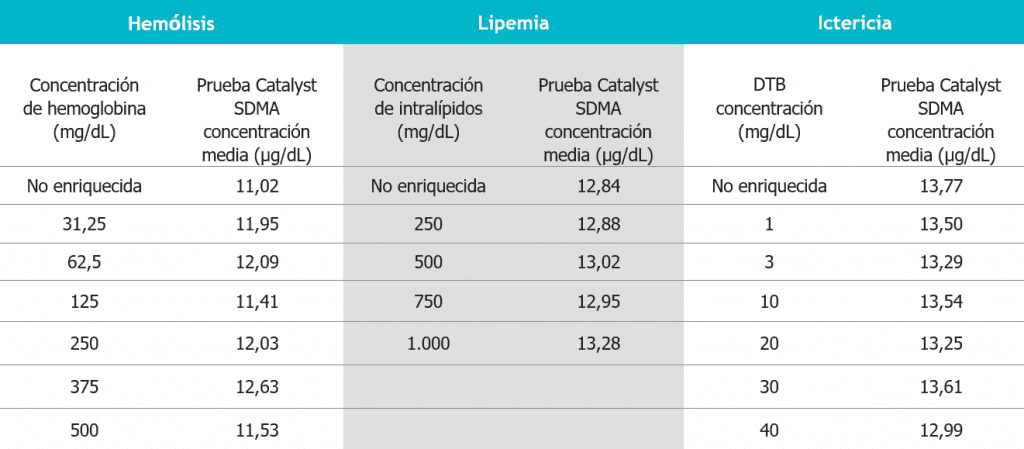
Los resultados del estudio de las substancias interferentes se muestran en la tabla 6. Las substancias interferentes comunes examinadas aquí no tuvieron un impacto estadísticamente significativo en las concentraciones de SDMA reportadas.
Tabla 6. Impacto de las sustancias interferentes.
CONCLUSIONES
La nueva Prueba IDEXX Catalyst® SDMA demuestra una excelente correlación con el método de referencia.
Ofrece a los veterinarios una opción exacta, precisa, fiable y cómoda para diagnosticar y monitorear a los perros y gatos con enfermedades renales mediante los analizadores químicos internos Catalyst Dx® y Catalyst One®.
REFERENCIAS
- Kielstein JT, Salpeter SR, Bode-Boeger SM, Cooke JP, Fliser D. Symmetric dimethylarginine (SDMA) as endogenous marker of renal function—a meta-analysis. Nephrol Dial Transplant. 2006;21(9):2446–2451.
- Nabity MB, Lees GE, Boggess M, et al. Symmetric dimethylarginine assay validation, stability, and evaluation as a marker for early detection of chronic kidney disease in dogs. J Vet Intern Med. 2015;29(4):1036–1044.
- Hall JA, Yerramilli M, Obare E, Yerramilli M, Almes K, Jewell DE. Serum concentrations of symmetric dimethylarginine and creatinine in dogs with naturally occurring chronic kidney disease. J Vet Intern Med. 2016;30(3):794–802.
- Braff J, Obare E, Yerramilli M, Elliott J, Yerramilli M. Relationship between serum symmetric dimethylarginine concentration and glomerular filtration rate in cats. J Vet Intern Med. 2014;28(6):1699–1701.
- Hall JA, Yerramilli M, Obare E, Yerramilli M, Jewell DE. Comparison of serum concentrations of symmetric dimethylarginine and creatinine as kidney function biomarkers in cats with chronic kidney disease. J Vet Intern Med. 2014;28(6):1676–1683.
- Hall JA, Yerramilli M, Obare E, Yerramilli M, Yu S, Jewell DE. Comparison of serum concentrations of symmetric dimethylarginine and creatinine as kidney function biomarkers in healthy geriatric cats fed reduced protein foods enriched with fish oil, L-carnitine, and medium-chain triglycerides. Vet J. 2014;202(3):588–596.
- Hall JA, Yerramilli M, Obare E, Yerramilli M, Melendez LD, Jewell DE. Relationship between lean body mass and serum renal biomarkers in healthy dogs. J Vet Intern Med. 2015;29(3):808–814.
- Zady MF. Z-stats/basic statistics, Z-12: Correlation and simple least squares regression. Westgard QC website. westgard.com/lesson42.htm. Published August 2000. Accessed December 5, 2017.
- Evaluation of Precision of Quantitative Measurement Procedures; Approved Guideline—Third Edition. CLSI document EP05-A3. Wayne, PA: Clinical and Laboratory Standards Institute; 2014.
- Patch D, Obare E, Prusevich P, et al. High throughput immunoassay for kidney function biomarker symmetric dimethylarginine (SDMA) [AACC abstract B-047]. Clin Chem. 2015;61(10):S135.
- Interference Testing in Clinical Chemistry; Approved Guideline—Second Edition. CLSI document EP7-A2.
Wayne, PA: Clinical and Laboratory Standards Institute; 2005.
- Prusevich P, Patch D, Obare E, et al. Validation of a novel high throughput immunoassay for the quantitation of symmetric dimethylarginine (SDMA) [AACC abstract B-048]. Clin Chem. 2015;61(10):S135.
© 2018 IDEXX Laboratories, Inc. Todos los derechos reservados. • 09-2077604-01 Catalyst, Catalyst Dx, Catalyst One e IDEXX SDMA son marcas comerciales o marcas registradas de IDEXX Laboratories, Inc. o de sus filiales en Estados Unidos y/o en otros países. Todos los demás nombres y logotipos de productos y empresas son marcas comerciales o marcas registradas de sus respectivos propietarios. La política de privacidad de IDEXX está disponible en idexx.com

